Produkty subskrypcyjne w twoim koszyku
Ustaw jedną częstotliwość dostaw dla wszystkich produktów subskrypcyjnych z twojego koszyka co:
Produkty subskrypcyjne w twoim koszyku
Glukoza dekstroza
Przejdź do nawigacjiPrzejdź do wyszukiwania
|
|||||
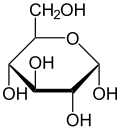
 α-D-glukopiranoza (projekcja stereochemiczna) |
|||||
|
|||||
| Ogólne informacje | |||||
| Wzór sumaryczny | C6H12O6 | ||||
|---|---|---|---|---|---|
| Masa molowa | 180,16 g/mol | ||||
| Wygląd | bezbarwne, drobne kryształki o słodkim smaku[1] | ||||
| Identyfikacja | |||||
| Numer CAS | 50-99-7 26655-34-5 (izomer α-D) 28905-12-6 (izomer β-D) 58367-01-4 (racemat) 77938-63-7 (monohydrat) |
||||
| PubChem | 5793 | ||||
| DrugBank | DB02379 | ||||
|
|||||
|
|||||
|
|||||
| Podobne związki | |||||
| Podobne związki | fruktoza, sorboza, galaktoza i inne heksozy | ||||
| Pochodne | glukozo-6-fosforan | ||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) |
|||||
| Klasyfikacja medyczna | |||||
| ATC | V04CA02, B05CX01, V06DC01, C05BB56 | ||||
|
|||||
Glukoza, D-glukoza (stgr. γλυκός glykós „słodki”, -oza przyrostek oznaczający węglowodany) – organiczny związek chemiczny, monosacharyd (cukier prosty) z grupy aldoheksoz. Jest białym, drobnokrystalicznym ciałem stałym[1], z roztworów wodnychłatwo krystalizuje jako monohydrat[7]. Jest bardzo dobrze rozpuszczalna w wodzie[1](nie zmienia pH roztworu). Ma słodki smak, nieco mniej intensywny od sacharozy[8].
Enancjomerem D-glukozy jest L-glukoza, niewystępująca w organizmach wyższych.
Występowanie
Glukoza powstaje w organizmach roślinnych podczas fotosyntezy[9]:
- 6H2O + 6CO2 + hν (energia świetlna) → C6H12O6 + 6O2↑; ΔE = −2872 kJ/mol (–687 kcal/mol)
- gdzie: h – stała Plancka ; ν – częstotliwość fali
Występuje w znacznych ilościach w owocach (szczególnie w winogronach, stąd nazywana jest czasem cukrem gronowym) i miodzie. W organizmach jest składowana w postaci dwóch polimerów: skrobi u roślin i glikogenu u zwierząt.
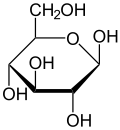
Budowa cząsteczki
Krystaliczna glukoza ma budowę cykliczną. Sześcioczłonowy pierścień hemiacetalupowstaje w wyniku reakcji grupy aldehydowejprzy atomie węgla C1 z grupą hydroksylowąprzy atomie węgla C5 w łańcuchu. Możliwe są zatem dwa anomery – α oraz β w zależności od położenia grupy OH przy pierwszym atomie węgla formy cyklicznej.
W roztworze wodnym oba anomery mogą ulegać reakcji otwarcia pierścienia i ponownego zamknięcia z utworzeniem ponownie takiego samego lub przeciwnego anomeru. Proces taki nazywa się mutarotacją. Forma otwartołańcuchowa występuje wyłącznie w roztworze wodnym, a jej termodynamiczna stabilność jest znacznie mniejsza od formy cyklicznej, dlatego równowaga procesu mutarotacji przesunięta jest silnie w kierunku formy cyklicznej, która występuje w przewadze.
W łańcuchowej formie glukozy znajdują się cztery asymetryczne atomy węgla (tj. C2, C3, C4 i C5), podczas gdy w formie cyklicznej występuje pięć takich atomów (dodatkowo asymetryczny jest węgiel anomeryczny, C1). W zależności od położenia grupy karbonylowej w łańcuchu i konfiguracji asymetrycznych atomów węgla, możliwych jest kilkadziesiąt izomerów glukozy (zob. heksozy). Jednym z często występujących naturalnie izomerów glukozy jest fruktoza, różniąca się położeniem grupy karbonylowej.
Właściwości
Właściwości chemiczne
Naturalna glukoza jest jednym z wielu izomerów optycznych tego związku – α-D-glukopiranozą (dekstrozą). Jest ona czynna optycznie – w temperaturze pokojowej skręca płaszczyznę spolaryzowanego światła białego w prawo. Skręcalność właściwaanomeru α wynosi +112°, natomiast anomeru β +19°. W roztworze wodnym w wyniku mutarotacji ustala się stan równowagi obu anomerów w stosunku 36:64, o skręcalności właściwej +52,6°[10].
Glukoza w przeciwieństwie do fruktozy odbarwia wodę bromową w obecności kwaśnego węglanu sodu[11] (następuje utlenieniegrupy aldehydowej do grupy karboksylowej, w wyniku czego powstaje kwas glukonowy)[1]:
- CH2OH−(CHOH)4−CHO + Br2 + 2NaHCO3 → CH2OH−(CHOH)4−COOH + 2NaBr + H2O + 2CO2↑
Pod wpływem kwasu azotowego grupa aldehydowa oraz atom węgla C6 są utleniane do grup karboksylowych, w wyniku czego powstaje kwas glukarowy (który w gorącej wodzie przechodzi w lakton)[1].
W temperaturze powyżej 150 °C topi się i brunatnieje, tworząc (podobnie jak sacharoza) karmel[1].
Właściwości biologiczne
D-Glukoza jest podstawowym związkiem energetycznym dla większości organizmów, przechowywanym pod postacią polimerów – skrobi i glikogenu. Stanowi cukier najłatwiej przyswajalny przez człowieka[1]. W procesie glikolizy jest rozkładana na kwas pirogronowy. Jest także substratem wielu procesów zachodzących w komórce, a u roślin, jako celuloza, podstawowym budulcem ściany komórkowej.